
1. 题目要素拆解

1)预测变量:病理组学特征
2)结局:Microsatellite instability(MSI)微卫星不稳定性
3)研究对象:结直肠癌(CRC)
2. 文章基本信息
3.核心要素
研究对象(P):结直肠癌(CRC)患者(TCGA-COAD,n = 429;Asian-CRC,n=785)研究目的:开发基于组织病理学图像的病理组学特征、用于预测结直肠癌(CRC)患者的微卫星不稳定性(MSI)模型
4.变量分析
5.研究背景
临床问题:微卫星不稳定(MSI)是一种高突变表型,发生在DNA错配修复缺陷(DNA mismatch repair deficiency,dMMR)的肿瘤中,是遗传性林奇综合征(Lynch syndrome,LS)相关癌症的重要标志,在约15%的结直肠癌中观察到MSI表型;更重要的是,MSI或dMMR与肿瘤增加的新抗原负荷相关,从而使其对免疫检查点阻断剂(immune checkpoint blockade,ICB)治疗敏感;进一步的研究表明,ICB治疗对MSI患者的获益不限于特定的肿瘤类型,因此MSI对于预测晚期实体瘤特别是CRC的免疫治疗疗效至关重要。
目前方法不足:临床上MSI或dMMR常规检测仅限于CRC和子宫内膜癌患者,并不是每个患者都进行了MSI检测;MSI需要额外的遗传或免疫组织化学检测,既昂贵又耗时;而且,现有的各种MSI检测方法具有不同的敏感性和特异性,导致结果不统一。本文解决方式:基于此,作者从组织病理学图像中构建MS状态预测模型,并识别关键的病理特征,将探索其与基因组和转录组等特征的相关性,以期为临床免疫治疗决策提供参考。
1. Work flow展示
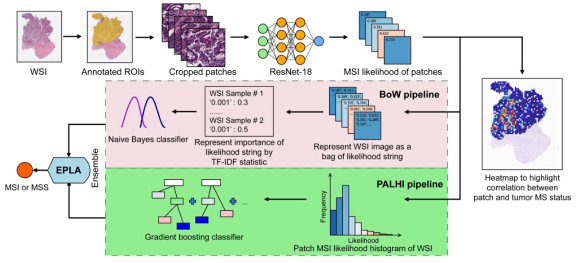 Figure 1
Figure 1
我们先来看一下流程图,Ensemble Patch Likelihood Aggregation(EPLA)模型的建立过程:①WSI进行注释以标注肿瘤区域(regions of carcinoma,ROIs);③输入ResNet-18以预测patch-level的MSI可能性;④分别通过PALHI和BoW pipelines(流程)将多个patch-level 对MSI的预测集成为WSI-level对MSI的预测;⑤最后,集成学习结合两种流程的结果,建立EPLA模型对MS状态进行最终预测。2.纳入排除标准建立
① TCGA-COAD队列:诊断为结肠腺癌(COAD),Stage I-IV期② Asian-CRC队列:诊断为结直肠癌(CRC),Stage I-IV期标本类型:冰冻切片(TCGA-COAD),福尔马林固定石蜡包埋的组织样本FFPE(Asian-CRC)MS状态:TCGA-COAD队列,MSI评分≥10的肿瘤定义为微卫星不稳定MSI(n=71),MSI评分<10定义为微卫星稳定MSS(n=429)(方法:使用MSIsensor算法基于肿瘤-正常配对基因组测序数据计算每个样本的MSI评分);Asian-CRC队列,5个微卫星位点中有2个以上不稳定的肿瘤被定义为微卫星高度不稳定型MSI-H(n=164),其余被定义为微卫星位点不稳定型MSI-L/微卫星稳定型MSS(n=621)(方法:采用MSI检测试剂盒基于多重PCR-毛细管电泳法检测5个微卫星位点(BAT-25, BAT-26, D5S346, D2S123和D17S250))。最终,共纳入TCGA-COAD队列429名患者和Asian-CRC队列785名患者,其中TCGA-COAD队列采用分层抽样,以7:3的比例分成单独的训练集(n=300)和测试集(n=129),以保持训练集和测试集中阳性和阴性样本的比例相同;Asian-CRC队列用于外部验证集。并从中获得病理特征、基因组及转录组测序数据。3.图像分割(+图像预处理)
所有WSI在预定像素分辨率(~0.5μm/像素)的20×物镜下进行数字化,由病理专家手动标注WSI中的肿瘤区域(ROI),原则如下:①肿瘤细胞应占ROI的80%以上,即间质成分小于20%;②排除明显干扰因素,如折痕、出血、坏死、模糊区域等。注释过程使用Aperio ImageScope软件。WSI以非重叠方式平均分割成512×512像素的patch,仅与ROI重叠区域超过80%的patch被纳入进行后续分析。TCGA-COAD中每个WSI的patch数量约为22-2357(平均为224个),而Asian-CRC中每个WSI的patch数量约为5-3718(平均为338个)。TCGA-COAD训练集patch进行数据增强和归一化处理,测试集patch只进行数据的归一化处理。数据增强是指对patch进行随机水平翻转和随机仿射变换(保持中心不变)的处理。最后,在RGB通道上进行z-score归一化后,将增强后的patch围绕中心裁剪为224× 224像素。补充:在深度学习(图像领域)中,对图像进行数据增强的方法有随机仿射变换、颜色抖动,水平/垂直翻转,弹性变换等,使得训练数据的分布更加复杂,以提高模型的泛化能力。4.预测模型建立
作者通过三步流程完成本文基于多实例学习(Multiple Instance Learning,MIL)的深度学习预测模型建立:①patch-level计算MSI可能性;②通过两种独立的MIL方法分别聚合(aggregate)patch-level对MSI的预测;③最终集成(ensemble)WSI-level对MSI的预测。首先,将上述处理后的patch投入到ResNet-18(残差卷积神经网络)中计算patch-level的MSI可能性。使用二元交叉熵损失(Binary cross-entropy loss,BCE loss)函数,采用小批量梯度下降法对网络进行优化。补充:ResNet系列网络,图像分类领域的知名算法,常用于图像识别任务。ResNet-18指的是,网络的基本架构是ResNet,网络的深度是18层(这里的网络深度指的是网络的权重层,包括池化,激活,线性层;而不包括批量化归一层,池化层)。补充:二元交叉熵损失函数是机器学习模块中二分类问题中常用的一个损失函数,用来评判一个二分类模型预测结果的好坏程度。图2A分别展示了MSI和MSS病例patch-level预测MSI的代表性热图。
 Figure 2
Figure 2
随后,通过两种独立的MIL方法来聚合patch-level预测MSI的可能性:Patch Likelihood Histogram(PALHI)和Bag of Words(BoW),分别受到基于直方图的方法和基于词汇的方法的启发。在PALHI算法中,用patch-level MSI预测可能性的直方图来表示WSI,并使用了梯度增强决策树——极限梯度增强(Extreme Gradient Boosting, xgboost)输出最终WSI-level MSI预测结果;在BoW算法中,将WSI图像视为多个patch-level MSI预测可能性的集合,将每个patch映射到一个TF-IDF浮点变量,并计算TF-IDF特征向量来表示WSI,然后将这些特征向量进一步纳入朴素贝叶斯分类器(Naïve Bayes,NB)来预测每个WSI的MS状态。最后,为了获得两种MIL方法的最优凸组合,使用集成学习建立EPLA模型,最终预测患者的MS状态。
1. 预测模型评价
建立EPLA模型后,在TCGA-COAD中进行了分类性能评估。1. EPLA模型在TCGA-COAD中区分度AUC达到0.8848(图2B);2. EPLA模型性能优于Kather等人研究的DL-based MV模型(Deep-Learning based Majority Voting method)(TCGA-COAD同一队列的比较:0.8848 vs 0.8457;与其原始队列TCGA-CRC-KR的比较:0.8848 vs 0.84)(图2C)。
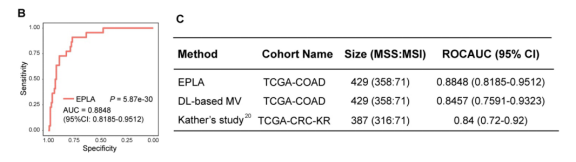 Figure 2
Figure 2
进一步比较了EPLA模型的两个组成部分(即PALHI和BoW)与DL-based MV模型的特异性和敏感性。1. PALHI在敏感性方面优于DL-based MV模型(86.4% vs 81.8%),BoW在特异性方面优于DL-based MV模型(89.5% vs 75.2%)。集成的EPLA模型结合了两种方法的优势,因此与DL-based MV模型相比,具有更高的特异性和敏感性(表S2)。
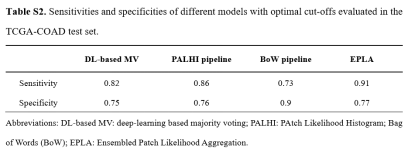
Table S2
2. 代表性的争议性病例如图S3所示,热图显示这些病例的EPLA模型MS状态预测正确,但DL-based MV模型预测错误。
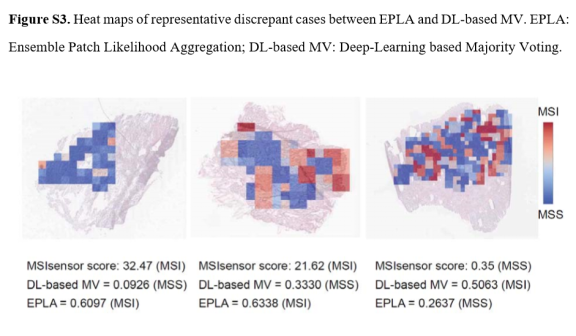 Figure S3
Figure S3
此外,还进行了探索性分析,以确定EPLA识别的病理表型。值得注意的是,EPLA捕获了分化程度(低、中或高分化)与MS状态之间的关系。MSIsensor评分较高或被EPLA模型预测为MSI的肿瘤表现出较高比例的低分化,MSIsensor评分较低或被EPLA模型预测为MSS的肿瘤表现为高分化和中分化的比例显著增加(P < 0.001),进一步证明了EPLA模型与病理形态之间具有内在联系(图2D)。
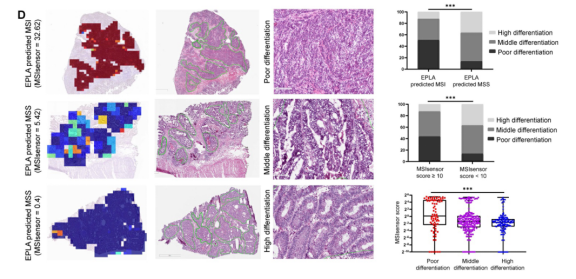 Figure 2
Figure 2
2.预测模型的外部验证
EPLA模型在外部验证数据集Asian-CRC中进行初步应用,评估其分类性能。EPLA模型在Asian-CRC队列中区分度AUC仅为0.6497(图3A)。
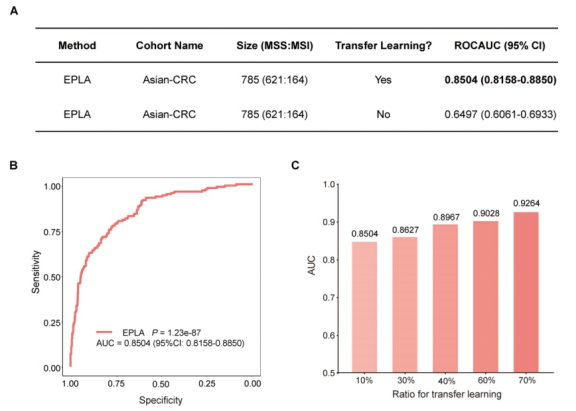 Figure 3
Figure 3
考虑到Asian-CRC和TCGA-COAD这两个队列不仅在患者种族上存在很大差异,而且在玻片制备技术上也存在很大差异。因此,在Asian-CRC队列中使用10%的病例对模型进行微调,应用迁移学习来推广EPLA模型。1. 应用迁移学习后该模型在Asian-CRC队列中的AUC达到0.8504(图3A-B);2. 随着应用于模型微调的患者比例逐渐增加,优化后的模型性能不断提高,在30%、40%、60%和70%的比例下,AUC分别为0.8627、0.8967、0.9028和0.9264。由此可见,迁移学习能够有效克服不同队列间的异质性带来的差异。3.生物学意义
为了深入了解EPLA模型的MSI预测机制,作者探索了EPLA模型在预测队列TCGA-COAD时的病理特征分布,按照病理特征对WSI-level水平MSI预测的权重进行排序,找出5个最重要的病理特征:FEA#197、FEA#198、FEA#001、FEA#188、FEA#200(图4A),并纳入后续分析。其中,FEA#001的值与MSS组显著相关(P < 0.0001),而其他4个(FEA#188/197/198/200) 则与MSS组显著相关(P < 0.0001) (图4B)。
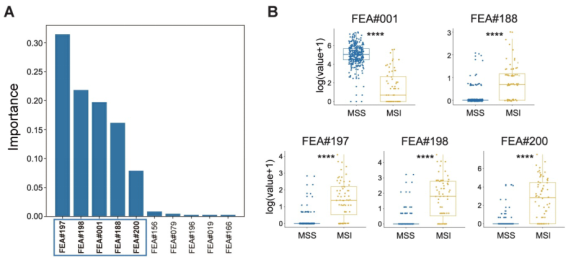 Figure 4
Figure 4
将上述5个重要的病理特征与TCGA-COAD基因组学数据进行相关性分析。
结果显示,FEA#001高的患者主要是MSS表型,表现为DNA修复相关通路功能正常,包括错配修复(mismatch repair,MMR)、DNA损伤响应与修复(DNA damage response and repair,DDR)、同源重组缺陷(homologous recombination deficiency,HRD);相反,FEA#188/197/198/200高的患者主要是MSI表型,存在DNA修复相关通路缺陷,即dMMR、dDDR和dHRD。另外,这些途径中几个代表性基因的突变,包括POLE、BRCA1和BRCA2,也发现了一致的结果(图4C)。由于最近的证据表明MSI与TMB(肿瘤突变负荷)显著相关,特别是INDEL(插入缺失)突变负荷。结果显示高TMB和INDEL突变负荷与低FEA#001和高FEA#188/197/198/200显著相关(图4C)。补充:由于TCGA-COAD突变数据是通过全外显子组测序得到的,TMB计算为整个基因组的体细胞非同义突变总数除以外显子区大小;INDEL突变是指由序列插入(INS)或缺失(DEL)引起的变异类型,可计算为INS和DEL突变的频率。
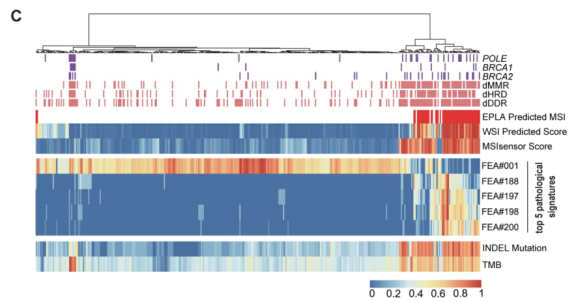 Figure 4
Figure 4
对TCGA-COAD的mRNA表达谱进行加权基因共表达网络分析(weighted gene co-expression network analysis,WGCNA),鉴定出24个转录组模块并进行GO富集分析,其中18个具有生物学功能的模块进行下一步分析(图5A)。随后将18个模块与5个重要的病理特征进行Spearman等级相关性分析,结果显示ME12、ME8、ME21、ME14、ME13、ME18和ME16这7个模块与FEA#001呈显著负相关,而与其余4个病理特征(FEA#188/197/198/200)呈显著正相关(图5B)。继而,通过对比相关模块中显著富集的GO项,发现富集ME13和ME8的分子主要与免疫激活的生物学过程有关,如T细胞激活和调节白细胞激活,富集ME12的分子则与炎症细胞因子信号转导相关的生物学过程有关,如IFN-γ介导的通路等(图5C)。从抗肿瘤免疫的角度进一步研究病理特征与转录组的相关性,分别从RNA-seq数据中计算出免疫细胞溶解活性(cytolytic activity,CYT)评分(即GZMA和PRF1转录水平的几何均值),和CD8+ T效应基因集(CD8A、IFNG、GZMA、PRF1、CXCL9、CXCL10、TBX21、GZMB)。结果显示,FEA#001与CYT评分呈显著负相关,FEA#188/197/198/200与CYT评分呈显著正相关,这与MSI患者CYT评分更高的结果一致(图5D);FEA#001与CD8+ T效应基因表达水平显著负相关,FEA#188/197/198/200与CD8+ T效应基因表达水平呈显著正相关,这也与MSI患者CD8+ T效应基因表达水平更高的结果一致(图5E)。综上所述,EPLA模型重要的病理特征在一定程度上反映了MSI的抗肿瘤活性,增强了免疫检查点抑制剂的疗效。
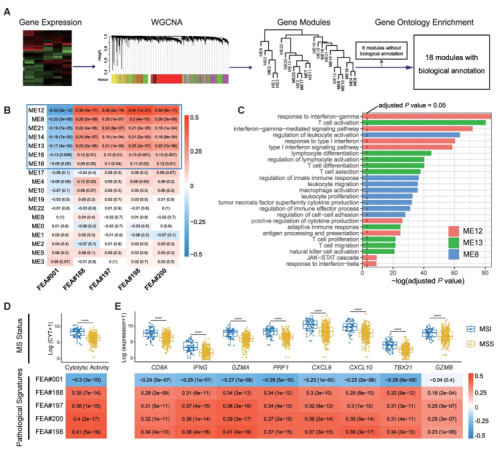
Figure 5
本文基于组织病理学图像直接建立MS状态预测模型,在不同患者群体中使用迁移学习进行模型泛化,并分别从基因组和转录组关联的角度探讨了模型的可解释性和临床应用价值。
优点
这篇20年发表的文章建立预测模型的套路并不复杂,那么能够冲上Q1的亮点究竟在哪里呢?我认为原因在以下几点:1. 本文通过深度学习以组织病理学图像特征预测基因层面MS状态的idea非常具有创新性,并将其建立的模型与此前Kather等人研究的模型进行对比,预测性能显著提升;2. 在建立预测模型过程中,本文通过两种独立的MIL方法分别建立patch级别对MSI的预测,再通过集成学习提取这两种方法的各自优势建立WSI级别对MSI的预测,使最终模型的建立更胜于任一方法,也为我们开展病理组学研究提供了思路。3. 在具有高度异质性的队列中,通过迁移学习提高模型的泛化能力,消除种族、制备技术和数据采集技术带来的差异,使得模型能够进一步推广至更复杂的群体中,值得大家学习;4. 最后分别从基因组和转录组关联的角度对病理特征建立的模型进行解释,增强该模型在临床实践中的应用价值。
局限性
1. 深度学习模型的性能在很大程度上取决于训练集的大小和质量,本文使用TCGA-COAD(n = 300)作为测试集,最终仍需要扩展训练数据来提高模型的准确性和泛化性;2. 虽然EPLA模型在TCGA-COAD和Asian-CRC队列中得到验证,但将其作为常规MSI检测手段应用于临床实践之前,还需要进行大规模的前瞻性临床试验。本研究使用在线的数据集和国内多中心数据进行挖掘,发到Theranostics这本杂志,着实让人羡慕不已。本文直接从病理图像获取信息,以病理组学的角度去预测基因层面MSI状态,或者预测其他分子水平的变化,免于复杂的遗传测序或传统的免疫组化手段,仍然还有很多值得挖掘的地方,紧跟病理组学潮流的小伙伴们可以发散一下思路,冲到1区不是梦! 好啦,本期的文献分享到这里,对于追求1区的小伙伴是不是一次新的机会呢?继续跟紧君莲数据库的平鑫而论专栏,我们下期见吧~~
Figure 1
Figure 2
Figure 2
Figure S3
Figure 2
Figure 3
Figure 4
Figure 4