
文/杨立雯 凤凰网《肿瘤情报局》特约撰稿员
核心提要:
1. 5月10日,英国宣布有不少于5名“三亲婴儿”出生。“三亲婴儿技术”也被称为“线粒体捐赠治疗”,该技术通过将健康女性捐赠者卵子与亲生父母的DNA结合,共同制造婴儿胚胎,以避免婴儿患上线粒体遗传病。值得注意的是,“三亲婴儿”体内超过99.8%的DNA都来自他们的亲生父母。
2. 线粒体病属于母系遗传,中国国内的发病率在1/5000上下,且尚无有效治疗方案。截至目前,研究人员已经发现了300多个可能导致线粒体病的致命性突变,而“三亲婴儿技术”是避免新生儿患上这类疾病的最佳解决方案。
3. 英国是现今世界上唯一批准“三亲婴儿技术”的国家,但全球第一位“三亲婴儿”却是由美国的一位华裔生殖医生在墨西哥操刀完成的。这名“三亲婴儿”出生于2016年,现已长到了7岁,身体各项指标都检测正常。此后,乌克兰的一家诊所也成功应用“三亲婴儿技术”帮助7名婴儿免受致命遗传病的困扰。直到2019年,“三亲婴儿技术”被应用于治疗不孕症,使得一名不育的女性成功怀孕。
4. 然而“三亲婴儿技术”仍然备受争议,失败的案例也仍在发生。人们除了认为这项技术过于昂贵,无法应用在大多数病人身上之外,还在担心三名父母所带来的伦理问题。还有人质疑这项技术的本质就是在制造转基因人。这使得“三亲婴儿技术”的未来发展十分敏感且备受争议。
英国首批一个爸两个妈“三亲婴儿”群诞生,这批婴儿据说可预防致命遗传疾病
在美国制造出首位一个爸爸、两个妈妈的“三亲婴儿”诞生7年后,英国宣布他们首批“生产”了不少于5名“三亲婴儿”。

5月10日,英国人类受精与胚胎学管理局证实,英国首个体内含有三人DNA信息的“三亲婴儿”已经诞生。这是英国于2015年首次批准“线粒体捐赠治疗”八年后,出生的首批“三亲婴儿”。为了保护婴儿的隐私,包括婴儿性别在内的所有信息依旧处于保密状态,但英国人类受精与胚胎学管理局表示:截至4月底,这批婴儿的人数不少于5名。

这种被称为“线粒体捐赠治疗”(MDT)的体外受精技术,使用来自健康女性捐赠者卵子与生育父母亲的DNA结合,一起制造婴儿胚胎,从而可以帮助生育母亲避免将基因退化疾病遗传给下一代。这个过程被命名为“三亲婴儿”,尽管婴儿中超过 99.8%的DNA来自母亲和父亲。

英国的这批“三亲婴儿”诞生并不是首例。据了解,自2012年开始,已有32名患者获准接受此类治疗。另据相关报道,这种仅用于遗传病治疗的技术,目前已应用到了患有不孕症的妇女群体。
英国人类受精与胚胎学管理局强调,目前线粒体捐赠治疗仍处于早期阶段,只有极可能将严重“线粒体疾病”遗传给子女的人,才有资格接受“线粒体捐赠治疗”。
从基因上来说,“三亲婴儿”有两个母亲一个父亲,但是捐赠线粒体的“母亲”和孩子的遗传联系较少。这意味着,这些孩子体内绝大部分的DNA(超过99.8%)依旧来自他们的父母,但还有大约0.1%的DNA和37个基因来自于第三位捐赠女性。
线粒体病是一种什么样的疾病?“三亲婴儿”真的可以解决遗传疾病问题吗?

▎2018年8月14日,伦敦南部Create Health生育诊所的一名胚胎学家在培养皿上工作。

什么是线粒体病?制造没有缺陷的“超人”是否有违伦理?英国议会为何会批准立法?
线粒体(mitochondrial)是真核细胞的“能量工厂”,存在于人体的几乎每一个细胞里。它的功能是将人体摄入的食物转换成能量。线粒体内有一套独立于细胞核的遗传物质。线粒体病属于母系遗传,一旦母体存在缺陷,可引起婴儿一系列广泛的健康问题,包括代谢性中风、癫痫、心肌病、发育或认知障碍、糖尿病、听力、视力、肝脏、胃肠或肾脏功能损害等。最新研究发现线粒体病可导致前列腺癌症。这些症状可以出现在任何年龄,从婴儿期到成年后期。目前尚无有效治疗方案。
▎有缺陷的线粒体。
对于线粒体病的研究已有九十多年的历史,1931年Alpers首先报道一例以大脑灰质受累为主的神经遗传性疾病,被称为Alpers病。1951年Leigh首先描述了以脑干对称性坏死为特点的一组疾病,被称为Leigh综合征。1958年Kearns和Sayre等报道了一例进行性眼外肌瘫痪伴随视网膜色素变性和心肌病的患者,被称为Kearns-Sayre综合征。1962年Luft等首次报道一例以骨骼肌极度不能耐受疲劳为特点的患者,生化研究证实为线粒体氧化磷酸化脱偶联引起,首次提出线粒体病的概念。在20世纪70年代,因为生化和酶组织化学技术的发展,Leigh综合征和Kearns-Sayre综合征被证实为线粒体病。▎通过来自健康女性捐献者卵子的组织制造没有母亲携带的有害突变的IVF胚胎。
截至目前为止,研究人员已经在300多个基因中发现了致病性的突变。纽卡斯尔大学的Doug Turnbull教授治疗线粒体疾病患者已有数十年,据他透露,在英国,大约每3000到5000人中就有1人患有线粒体疾病。而据相关数据,线粒体病在中国的发生率为1/5000。
由于线粒体DNA是从母亲遗传给后代,为避免因线粒体DNA缺陷而产生有遗传病的后代,科学家们提出了线粒体替代疗法(mitochondrial replacement therapy, MRT),就是用健康女性的卵细胞线粒体代替有缺陷的线粒体,母亲卵子的细胞核DNA加上父亲精子的DNA,构成一个完整的胚胎。也就是说,新生儿将有三位生物学父母:两位母亲,一位父亲。这一超前的体外受精技术首先在英国进行了合法化的试验。英国议会在2015年2月3日就是否允许“三亲婴儿”出生进行决定性表决,结果以382票赞成,128票反对获得通过。这是世界上至今唯一一个批准“三亲婴儿技术法案”的国家。此后,英国纽卡斯尔生育中心于2017年获得了第一个饱受争议的治疗许可。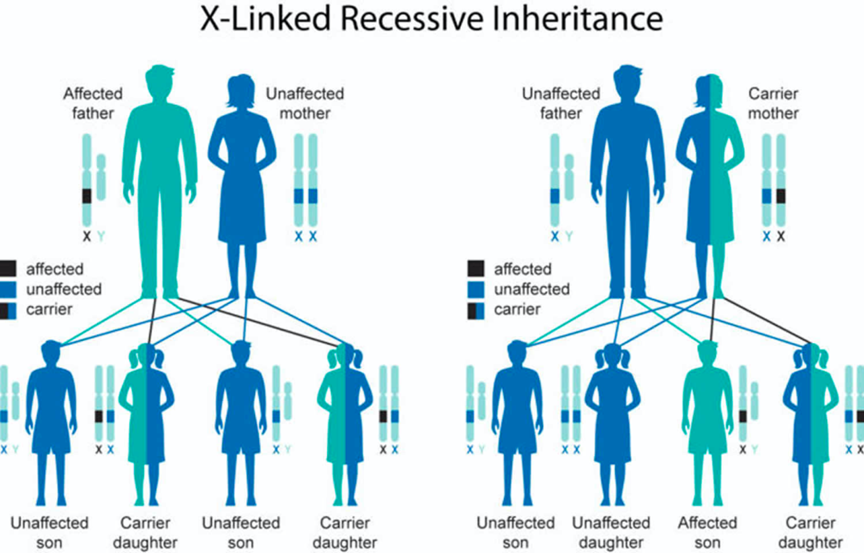

华裔医生创造了世界首个“三亲婴儿”,至今已7岁
英国虽然是全球第一个批准了“三亲婴儿技术法案”的国家,但全球第一位“三亲婴儿”的诞生,却在墨西哥,由美国的一位华裔生殖医生为这位母亲进行了首次“线粒体移植”。
这位名叫阿卜拉希姆·哈桑的孩子,生于2016年4月6日,今年已经7岁。这也是这种“三亲婴儿移植方法”在人类身上使用的历史。
2016年9月,这个男婴的主治医生团队在美国《生育与不孕》杂志上发表学术论文,公开了他的出生过程。文章披露,这位“三亲婴儿”的的母亲来自约旦,是一位Leigh综合征患者。她身上四分之一的线粒体携带有亚急性坏死性脑病的基因,这使得她生育的孩子无法正常发育,导致4次流产,即使是幸运生育下来两个孩子,也相继因该遗传病在8个月和6岁时去世。Leigh 综合征在这个家庭的遗传谱系里成为了难以避免的母系遗传病。目前没有有效的治疗方法,医生大多建议这种疾病患者直接放弃生育,以免忍受丧子之痛。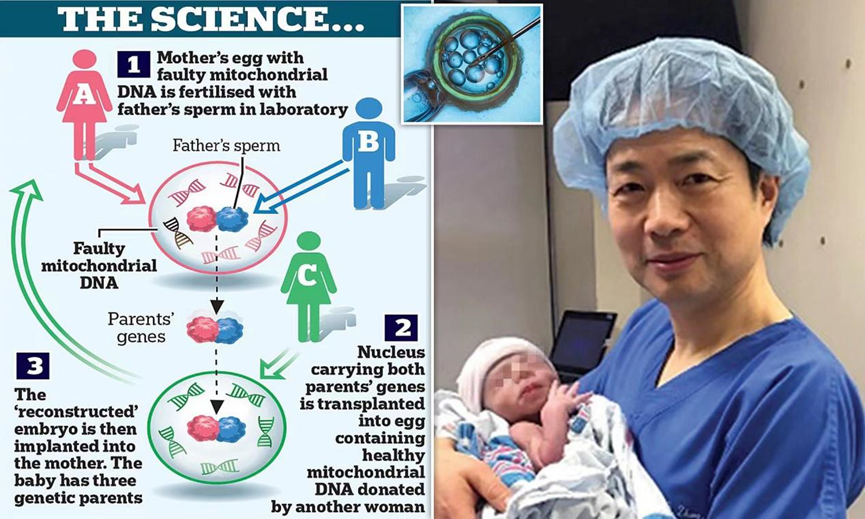
他们找到了美国纽约新希望生殖中心,该中心由美籍华人医生张进(John Zhang)于2004年创建,张医生1984年在浙江大学获得学士学位后到英国留学,在伯明翰大学和剑桥大学取得硕士学位和博士学位,之后前往美国,成为试管婴儿领域公认的顶级专家,在辅助生殖方面具有丰富经验。张医生提出了这项即使在7年前也仍为大胆的方案——“线粒体替代疗法”。张医生一直在研究使用所谓的“三亲技术”来避免线粒体疾病的方法。从理论上讲,“线粒体替代疗法”的主要方案有三种,原核移植、纺锤体移植和极体移植。英国批准的方法称为原核移植。但这种技术并不适合这对夫妇——作为穆斯林,他们反对破坏两个胚胎。所以张医生采取了纺锤体移植。即在受精前进行,将母亲的卵子中的纺锤体复合体提取出来,移植到供体相应的卵母细胞中,再进行受精。这个婴儿除了拥有父母的细胞核基因,还拥有捐赠女性的线粒体DNA。由于美国尚未批准线粒体替代疗法,张进医生团队和这对中东夫妻最终选择前往墨西哥,并获得了墨西哥诊所内部审查委员会的特别批准。 这名约旦孕妇怀孕37周后产下了这名男婴,根据检测,婴儿体内各组织细胞的线粒体变异比例各不相同,介于2.36%-9.23%,但一般线粒体疾病发病需要变异达到20%以上,所以这是一名健康的孩子。
2017年1月5日,乌克兰一名妇女成功生下一名拥有3位父母遗传基因的婴儿,成为世界上第二个“三亲婴儿”。与上一个“三亲婴儿”不同的是,该婴儿在生育过程中采用的是英国批准的“原核移植”技术。该技术用另一位卵子捐赠者的正常线粒体替换了“亲妈妈”不健康的线粒体,相当于把母亲、父亲和捐赠者三个人的细胞拼到了一起。因此,生出来的婴儿也就有了三种基因。报道证实,到目前为止,帮助这名乌克兰妇女生育的Nadiya诊所已经有7名婴儿出生。2019年4月9日,希腊诞生了一名同样被冠以“世界第一”头衔的“三亲婴儿”。但这名孩子的诞生并非为了治疗遗传疾病,而是为了治疗不孕症。他的母亲没有任何线粒体疾病,他的医生使用纺锤体移植技术,使她成功怀孕。替代疗法是生殖技术的一个重大突破,被称为第四代试管婴儿技术。这一移植方法,理论上将会成为不孕症的福音。
▎2016年,张进医生因完成世界首例“三亲婴儿”而入选Nature 2016年度十大科学人物,但在2017年论文发表后,FDA向张进发出警告信,要求他及所在诊所停止对这种技术的进一步宣传。
第四代试管婴儿技术其实是基因编辑?中国为何至今无类似研究?
“三亲婴儿技术”尽管成功的案例很多,但失败的案例仍然在发生。这项前沿技术在1990年代,差点引发人道灾难。其安全性与伦理至今仍备受争议。据《新科学家》杂志报道,美国一家诊所的医生试图使用三个人的DNA来创造婴儿,结果两个胎儿仍然出现了遗传疾病,这项技术随即被FDA制止。2014年6月,英国生育监管机构曾在一份报告中表示,根据三个人的DNA制造胚胎的有争议的技术“似乎并不安全”。FDA至今仍未批准这项有争议的试管婴儿技术。对于线粒体捐赠治疗,舆论褒贬不一。争论大多集中在这项技术价格昂贵,大多数病人如无经济援助,仍无法实施。同时“三亲婴儿”可能会经历与捐赠者之间令人困惑的关系,捐赠者可能被认定为“第二母亲”或“第三父母”。作为生物学层面的遗传贡献者,捐赠者可能会在未来声称自己是父母,这使其成为一个不可预知的风险。而这项技术本身,至今也仍然不成熟。许多批评人士反对人工生殖技术,认为还有其他方法可以避免将疾病传给孩子,比如卵子捐赠或筛查测试,而且这些实验方法尚未被证明是安全的。而对于这个所谓的“三亲婴儿”伦理的担忧与所谓可能创造出超人的担忧,一度成为人们争论的焦点。英国纳菲尔德生物伦理委员会主任休·惠托尔认为,“三亲婴儿”的说法具有误导性,不恰当,也无益,因为来自捐赠者线粒体的基因只有37个。父母细胞核DNA遗传的基因超过2万个,所以线粒体基因的作用几乎可以忽略不计,而且线粒体基因甚至远远低于通过输血或器官移植获得的捐赠者基因。整体而言,提供细胞核基因的父母决定了后代99.8%的基因,只有0.1%的基因由捐赠线粒体DNA的女性提供,“三亲婴儿”的相貌、血型、染色体、性格等基本特征只会遗传自自己的父母。这项被称为第四代试管婴儿的先进技术,实质上是一种生殖细胞的基因治疗技术,可视作一次对人类细胞的“转基因”——将母亲有遗传病基因的线粒体更换,达到阻断疾病遗传、优生优育的目的。
有反对者撰文认为,这事实上是在制造转基因人。一些批评者认为,这项技术的本质就是人造胚胎,相当于“设计”新生儿。依赖这种技术,研究人员可以对胚胎实施基因改造,以干预新生儿的发色和成人后的身高。这是首次母体遗传DNA“种系”发生改变,标志着试管婴儿伦理道德的转折点。而参与研究的科学家辩解说,额外的线粒体DNA片断并不参与婴儿的基因重组与改造,而且这种“无害”的遗传物质不会影响到正常的智力、性格发育,因此,这批婴儿的基因和基因组并未被修改,不能称其为“转基因婴儿”。
2018年,南方科技大学副教授贺建奎宣布将基因(CCR5)经过修改后,可以天然抵抗艾滋病病毒HIV的双胞胎出生,引发伦理争风波并获刑。我国也制订了“将基因编辑、克隆的人类胚胎植入人体或者动物体内,或者将基因编辑、克隆的动物胚胎植入人体内,情节严重的,处三年以下有期徒刑或者拘役“的刑法新条例。据了解,目前国内“三亲婴儿技术”的研究,仍处于个案研究。至今无正式的临床试验开展。