根据scRNA-seq数据,寻找差异数据,得到signature来对预后进行分析是生信常见套路,也是发文高分热门领域之一。但越来越多的小伙伴加入这个套路后,发文会越来越卷,稿件接收要求会水涨船高,也是可以预见的事。但如果想给自己的单细胞文章增加一个新方向呢?细胞间的差异数据类型可以是不同的,引发差异的原因也可以是不同的。只需要换一换科学问题,套路都是一样的。很多前几期文章用的新方法也可以组合进来。
输入signature ferroptosis,不仅文章发表趋势仍在持续增长,而且绝大多数都是去年和今年才发表,一共454篇,今年就发表了247篇,占据了一半以上!再按出版时间看看小伙伴们最新发表的文章,最少也都在5+或6+。可见,如果做单细胞signature,加个细胞死亡,相当一段时间内还是大有可为的。
下面我们就根据2篇最近一个月5+文献整理一下研究套路,看看如果我们现在就动手准备,最保底能发几分的文章!Yao W, Liu X, He Y, Tian M, Lu S, Wang Q, Zheng Y, Lv Z, Hao C, Xue D, Meng X. ScRNA-seq and bulk RNA-seq reveal the characteristics of ferroptosis and establish a risk signature in cholangiocarcinoma. Mol Ther Oncolytics. 2022 Sep 26;27:48-60. (IF=6.331)
Zhang Y, Liang Y, Wang Y, Ye F, Kong X, Yang Q. A novel ferroptosis‑related gene signature for overall survival prediction and immune infiltration in patients with breast cancer. Int J Oncol. 2022 Dec;61(6):148. (IF=5.884)
GSE138709 5个肿瘤组织、3个邻近组织、33694个基因和40919个细胞 CHOL scRNA-seq数据。GSE107943 30个CHOL样本,27个癌旁组织 RNA测序数据和临床信息TCGA-CHOL 36个CHOL和4个癌旁组织 RNA-seq数据和相应的临床信息。关于铁死亡的研究套路,我们也可以归纳到“挑圈联靠”的套路里。一、不同免疫细胞的比例(挑,选出预后最好的免疫细胞)为了评估各种免疫细胞浸润在组织细胞中的作用,利用RNA-seq数据分析了免疫细胞的比例及其对癌症预后的影响。CIBERSORT根据TCGA数据库的RNA-seq数据预测22种免疫细胞的比例(图1A)。研究者又对22种免疫细胞做了生存分析,单核细胞(Monocyte)的患者预后更好(P = 0.01)(图1B)。所以,研究者对癌和癌旁组织中单核细胞的浸润情况做了进一步。二、scRNA-seq分析表明单核细胞和CHOL细胞之间的交流(挑、圈、联)使用tSNE对scRNA-seq数据集(GEO: GSE138709)进行降维聚类,形成22个聚类(图2A),划分细胞亚群。图2B的热图显示每个细胞亚群的标记基因,依此对组织细胞(聚类0、2和5;标记物STMN1、KRT19和CLDN4)和符合研究者要求的免疫细胞——单核细胞(聚类3;标记物S100A9、S100A8和LYZ)进行分类(图2B)。图2D的点图展示了单核细胞和组织细胞之间相互作用,发现TNFSF13B和TFRC之间的关系是显著的(P<0.01)。TNFSF13B_TFRC对的出现次数在排名前30的细胞间关系对中排名第21位,足以说明其高频率(图2E)。对细胞亚群的标记基因进行了KEGG功能富集分析,但明显富集的途径不包括铁死亡途径(图2F)。样本中单核细胞和组织细胞之间的细胞间交流分析(图2C)显示了单核细胞浸润对组织细胞的影响。细胞通讯热图显示,胆管细胞(组织细胞)和内皮细胞之间的交流通讯最为突出。第二个最突出的通信是胆管细胞和单核细胞、巨噬细胞之间。在这里,一边挑选差异,一边做功能富集,“挑”的同时“圈”,因为我们要落实到不同细胞间功能的不同。
组织细胞的功能富集中没有发现TFRC相关的铁死亡信号通路,接下来研究者继续对组织细胞的细胞亚群重新进行细分,做tSNE图,重新得到9个亚群(图3A)。根据从KEGG数据库检索到的铁死亡基因signature的热图,铁死亡基因在C0、C1、C3、C4、C5、C7和C8中的富集程度较高,TFRC基因在C4亚群中明显过表达。铁死亡基因在C2和C6中的富集程度明显降低,TFRC基因在C6亚群中明显表达不足(图3C)。CNV分析显示,C0、C1、C3、C4、C5、C7和C8的拷贝数突变程度较高,表明它们是恶性细胞亚群。C2和C6的拷贝数突变程度较低,表明它们是良性的细胞亚群(图3D)。
研究者对C4(图3E)和C6亚群(图3F)的标记基因进行了KEGG功能富集分析。C4中的大部分通路与癌症直接相关,而C6中的通路与癌症没有直接关系,验证了从CNV推断的细胞亚群的良性和恶性鉴定结果。基于TFRC在C4中明显高表达而在C6中明显低表达,研究筛选了所有在C4中明显上调而在C6中明显下调的基因进行功能富集分析,结果显示,其中铁死亡的富集程度排在第五位(图3G)。
这些结果表明,与良性细胞相比,铁死亡途径在组织细胞中明显富集;单核细胞通过与组织细胞(TNFSF13B-TFRC)的交流,启动了部分癌细胞群的铁死亡。
为了进一步探索单核细胞在组织中的潜在作用,对TCGA数据进行WGCNA分析,构建共表达网络,确定共表达模块(图4A和4B),图B展示网络拓扑结构的性质,
分析不同模块与单核细胞(免疫细胞)高浸润和低浸润比例之间的相关性(图4C)。深绿松石色和棕褐色模块(共552个基因)与单核细胞浸润显著相关(P < 0.05),结果显示与高浸润呈负相关,与低浸润呈正相关。从FerrDb数据库中获得与铁死亡相关的基因。铁死亡相关的基因、单核细胞相关基因与差异表达的基因集相交,然后进行合并,做火山图(图4D),获得与铁死亡或单核细胞浸润的基因集交集,做维恩图(图4E)。对这些基因进行单变量Cox分析,筛选出单核细胞和铁死亡相关的基因(P<0.05),共9个基因。(图A)再对这9个与预后相关的基因进行多变量Cox回归分析,构建了一个三基因的预后signature。(图B)再对这三个基因及其相关基因三个基因的蛋白质-蛋白质相互作用网络,显示蛋白作用间的关联。根据这三个基因的表达值和相关系数,计算出每个患者样本的预后风险得分。
图5D和5E显示了TCGA-CHOL和GEO两个数据集分别的总风险得分(上图)、生存时间(中图)和单基因表达水平(下图)。
根据图5D和5E中显示的每个病人的风险评分,用最佳截止值将病人分为高风险组和低风险组。
接下来验证signature的临床效果,也同样是“靠”为了验证铁死亡-单核细胞(F-M)signature在不同数据平台上的预后性能,我们使用TCGA-CHOL作为训练集,GSE107943作为验证集。图6A和6C分别是TCGA-CHOL和GSE107943中高风险组和低风险组的KM生存曲线。在两个数据集中,CHOL患者的生存结果都有明显的不同(对数等级P<0.01)。ROC曲线被用来评估F-M特征对患者预后的敏感性和特异性。结果显示,TCGA-CHOL数据集表现更好,1年、3年和5年的曲线下面积(AUCs)分别为0.866、0.869和0.933(图6B)。GSE107943数据集的1年、3年和5年的AUC分别为0.618、0.792和0.910(图6D)根据TCGA数据的临床数据,使用决策曲线分析(DCA)重新评估了该预后特征在预测1年、3年和5年生存率方面的表现。结果显示,F-M特征在1年、3年和5年内比其他临床信息有更好的预测能力(图6E-6G)。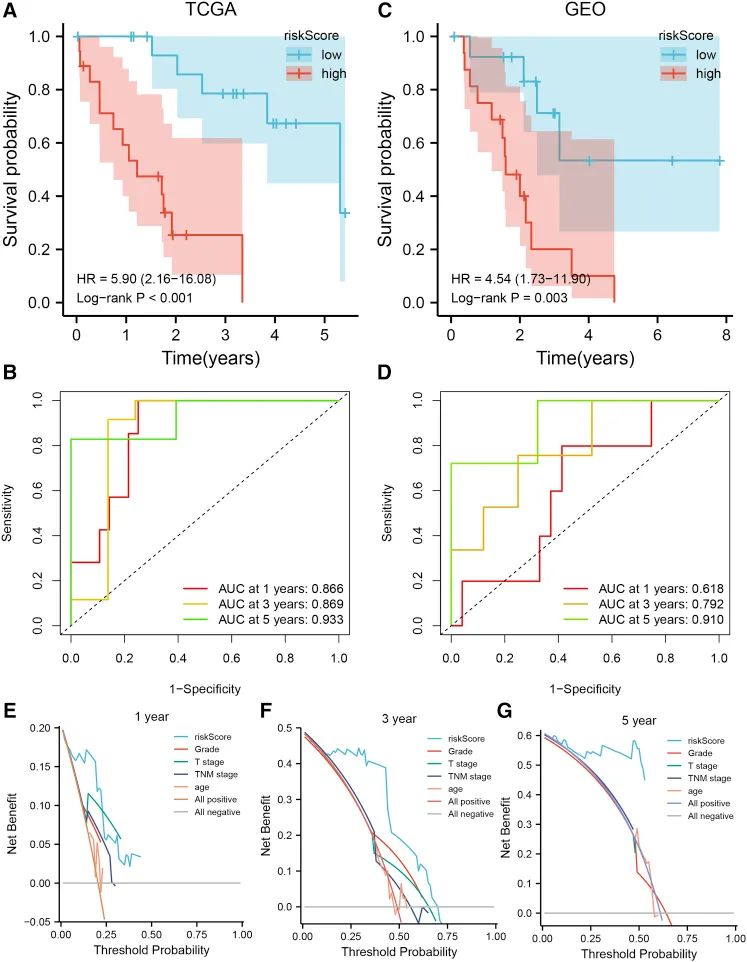
七、基于K-M生存分析和GSEA的列线图signature的构建(靠、圈)为了评估signature的应用潜力,我们将风险评分整合入列线图(图7A)。校准曲线显示,实际观察值与预测值很一致(图7B)。事实上,提名图风险评估图还可以将风险评分与临床特征相结合,以达到更好的临床应用价值。在基于基于单基因的KM曲线生存分析(图7C-7E)中,三个基因的低表达组有较好的预后,其中BNIP3和TMEM107有明显的预后效果,有一定的能力来区分患者的生存时间。根据F-M特征的中值,将TCGA-CHOL数据分为高分组和低分组,进行基于KEGG途径的基因集富集分析(GSEA),以获得可能参与F-M特征中三个基因调控的途径。(图7F-图7G)。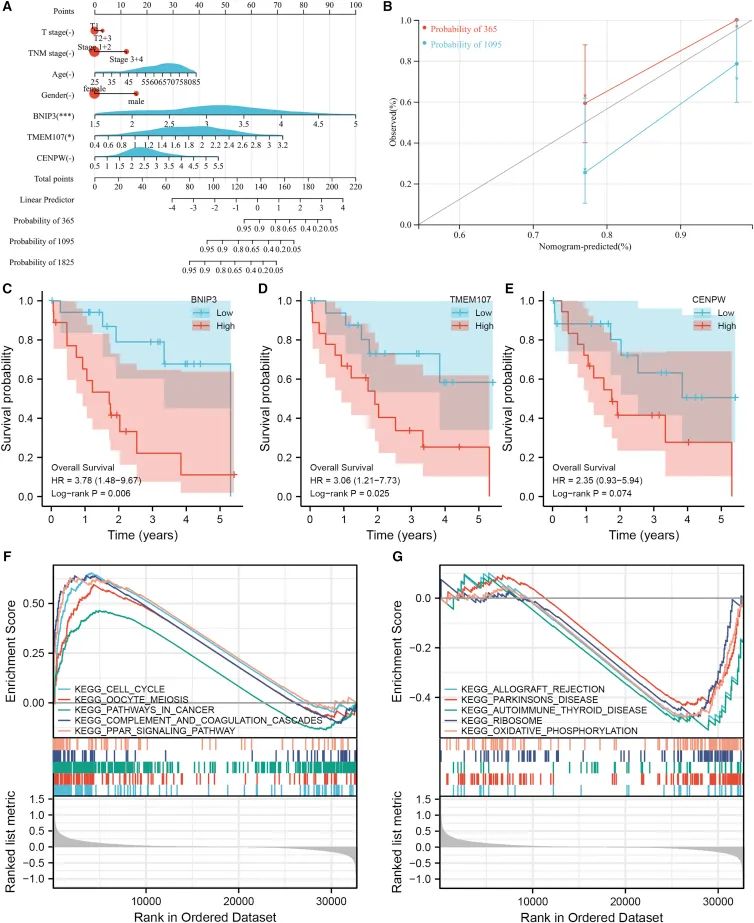
关于根据铁死亡相关基因筛选signature的文献套路就给大家介绍到这里了!和以往的基因signature套路一样很好发高分!各种高大上的新名词,只要能影响组织细胞,几乎都能轻松套用!单细胞signature
扫码立即咨询

—END—
撰文丨三叶虫
排版丨三叶虫
编辑丨三叶虫