来源:深究科学
作者:周晨

因两个孩子患有先天性糖尿病,哈佛学者开发干细胞疗法,有望治愈I型糖尿病,图片来Harvard大学
导读
I型糖尿病常常要求患者终身注射胰岛素治疗,尽管这能维持血糖水平,提高患者生活质量,但它并不能从根本上治愈这一疾病。
哈佛大学干细胞研究所联合主任道格拉斯·梅尔顿(Douglas Melton)的研究为I型糖尿病患者燃起了希望之光:他们开发一种干细胞替代疗法,与免疫抑制疗法联合使用,已在1/2期临床试验中,成功帮助首位患者再生其自身完全分化的胰岛细胞,这一突破性消息被认为可能会为I型糖尿病的治疗带来全新的前景。
梅尔顿之所以对I型糖尿病领域感兴趣,源于他的儿子和女儿先后均被诊断为I型糖尿病。作为父亲的他,转变了自己的研究方向,力求通过干细胞疗法帮助他的两个孩子。
今年6月底,Vertex公布了其基于干细胞的疗法 VX-880 的 I/II 期临床试验随访数据,显示在治疗后,两名I型糖尿病患者不再需要注射胰岛素,连续血糖监测还显示,两名患者 95% 的时间都处于血糖水平目标范围内。
“这些数据代表了I型糖尿病潜在治疗的突破性进展,使我们距离为正在等待的患者提供潜在的治愈疗法又近了一步。”
VX-880是一种异体干细胞疗法,可提供完全分化且能产生胰岛素的胰岛细胞,以恢复人体产生胰岛素。Vertex是收购了梅尔顿创立的公司Semma,而进入I型糖尿病领域。
本文为梅尔顿在Gazette上面的一次访谈,探讨了这一进展背后的科学故事,以及未来所面临的挑战。
梅尔顿:1920年,I型糖尿病治疗产生了第一个重大变革,那就是发现胰岛素。目前距离第一次重大变革已经过去了100多年。如果这项技术奏效,那将改变目前糖尿病患者的医疗治疗方式。患者将不再需要注射胰岛素,而是可以得到充当自己胰岛素生产工厂的细胞。这是一种新型药物。梅尔顿:近20年前,我们孕育了一个愿景:利用胚胎干细胞制造功能性胰岛细胞来治疗糖尿病。这项研究构想的初衷在于我们想弄清“人体内的胰岛细胞是如何不断进行自我补充的”。以血液为例,血干细胞会定期补充血液,就好像你参加献血活动时,你的体内就会自动产生更多血液。然而,我们在小鼠身上的研究却发现,对于胰岛细胞来说情况并非如此,一旦它们被移除或杀死,成年体内便无法再生新的胰岛细胞。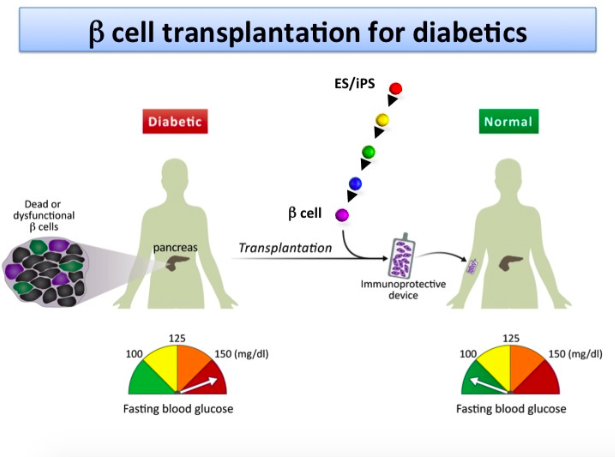 干细胞疗法产生新的胰岛细胞,或将治愈I型糖尿病正因如此,我们首要的“顿悟”时刻便是证明成年人无法自行产生新的胰岛细胞。这一认知引导我们转向另一种新材料:干细胞。然而,在克服围绕胚胎干细胞使用的障碍后,我们又面临着另一个重要问题:我们是否能够引导干细胞分化,使其成为β胰岛细胞?这一难题比我最初预计的耗时更长。我曾告诉我的妻子或许需要5年时间,但实际上却接近了15年。这项研究得益于本科生、研究生以及博士后研究员的参与,尽管他们不会连续为这项研究工作15年,但他们在不同的研究阶段都作出了卓越贡献。梅尔顿:这项工作绝对无法仅凭传统的国家卫生研究院(NIH)的支持而完成。首先,NIH的资助带来了相当严格的限制;其次,像这样一个长期的项目并不容易与他们最初为一到三年的项目提供的初始资助相匹配。因此,对于哈佛干细胞研究所的慷慨支持,我感激不尽,也感到幸运,因为这个研究所通过慈善捐款不仅提供了实质性的帮助,而且起到了至关重要的作用。我还特别感激前哈佛大学校长拉里·萨默斯(Larry Summers)和布罗德研究所斯坦利精神研究中心主任史蒂夫·海曼(Steve Hyman)。正是他们支持了哈佛干细胞研究所的创建,该研究所的设立旨在专注于多能干细胞的潜力,用以解答关于发育机理、细胞生成过程以及为疾病寻找新疗法和治疗方式的诸多问题。这项技术可能是这一构想首次得以实现的一个范例。当时,使用胚胎干细胞引发了极大的争议,而史蒂夫和拉里则表示,这恰恰是他们愿意支持的科研领域。问:这项胰岛细胞工作被哈佛设置专利,并授权给您的生物技术公司Semma,该公司被Vertex收购。您能解释一下这如何反映了您与这项研究的个人关系吗?梅尔顿:Semma公司以我两个子女的名字——Sam和Emma命名而来。如今他们已经成年,却都患上了I型糖尿病。我的儿子在只有6个月大时被确诊患病。那时,我改变了我的研究方向,而比我儿子大四岁的女儿,在大约10年后,也就是14岁时被诊断出患上了糖尿病。当我儿子被诊断患病时,我对糖尿病一无所知,此前我一直在从事蛙的发育研究。但在我儿子确诊糖尿病后,我改变了研究方向,因为像所有的父母一样,我想着,“我该如何应对?” 当然,这也再次凸显了哈佛的灵活性。在那时,没有人会责问:“为何要调整你的研究计划?”梅尔顿:首次投入患者体内的干细胞替代疗法细胞需要与一类被称为免疫抑制剂的药物联合使用,这些药物可以抑制患者的免疫系统。这样做的原因在于,这些细胞并不来自患者自身,因此不被认为是“本体”。如果没有免疫抑制剂的干扰,这些细胞将遭到排斥。我们的目标是找到一种通过基因工程制造的细胞,能够避免被视为外来物。我坚信这是一个可以解决的问题。为什么?当一个女人怀孕生下一个孩子时,这个孩子拥有两套基因,一套来自母亲的卵子,这些基因被身体认定为“自己的”;另一套来自父亲,这些基因则被视为“非自己的”。然而,母体的身体为何不会对胎儿产生排斥反应呢?如果我们能够找到这其中的奥秘,将有助于我们思考如何在干细胞衍生的胰岛细胞中进行基因改造,使其能够适用于任何人体。这种技术不仅关乎糖尿病,还可以应用于其他任何需要移植的细胞,包括肝脏甚至心脏,这可能意味着我们将不再需要担心免疫抑制的问题。1.Breakthrough within reach for diabetes scientist and patients nearest to his heart.The Harvard Gazette.2.Douglas A. Melton, Ph.D. Harvard University.3.Can Lab-Grown Beta Cells Revolutionize Diabetes Care?.University of California San Francisco.
干细胞疗法产生新的胰岛细胞,或将治愈I型糖尿病正因如此,我们首要的“顿悟”时刻便是证明成年人无法自行产生新的胰岛细胞。这一认知引导我们转向另一种新材料:干细胞。然而,在克服围绕胚胎干细胞使用的障碍后,我们又面临着另一个重要问题:我们是否能够引导干细胞分化,使其成为β胰岛细胞?这一难题比我最初预计的耗时更长。我曾告诉我的妻子或许需要5年时间,但实际上却接近了15年。这项研究得益于本科生、研究生以及博士后研究员的参与,尽管他们不会连续为这项研究工作15年,但他们在不同的研究阶段都作出了卓越贡献。梅尔顿:这项工作绝对无法仅凭传统的国家卫生研究院(NIH)的支持而完成。首先,NIH的资助带来了相当严格的限制;其次,像这样一个长期的项目并不容易与他们最初为一到三年的项目提供的初始资助相匹配。因此,对于哈佛干细胞研究所的慷慨支持,我感激不尽,也感到幸运,因为这个研究所通过慈善捐款不仅提供了实质性的帮助,而且起到了至关重要的作用。我还特别感激前哈佛大学校长拉里·萨默斯(Larry Summers)和布罗德研究所斯坦利精神研究中心主任史蒂夫·海曼(Steve Hyman)。正是他们支持了哈佛干细胞研究所的创建,该研究所的设立旨在专注于多能干细胞的潜力,用以解答关于发育机理、细胞生成过程以及为疾病寻找新疗法和治疗方式的诸多问题。这项技术可能是这一构想首次得以实现的一个范例。当时,使用胚胎干细胞引发了极大的争议,而史蒂夫和拉里则表示,这恰恰是他们愿意支持的科研领域。问:这项胰岛细胞工作被哈佛设置专利,并授权给您的生物技术公司Semma,该公司被Vertex收购。您能解释一下这如何反映了您与这项研究的个人关系吗?梅尔顿:Semma公司以我两个子女的名字——Sam和Emma命名而来。如今他们已经成年,却都患上了I型糖尿病。我的儿子在只有6个月大时被确诊患病。那时,我改变了我的研究方向,而比我儿子大四岁的女儿,在大约10年后,也就是14岁时被诊断出患上了糖尿病。当我儿子被诊断患病时,我对糖尿病一无所知,此前我一直在从事蛙的发育研究。但在我儿子确诊糖尿病后,我改变了研究方向,因为像所有的父母一样,我想着,“我该如何应对?” 当然,这也再次凸显了哈佛的灵活性。在那时,没有人会责问:“为何要调整你的研究计划?”梅尔顿:首次投入患者体内的干细胞替代疗法细胞需要与一类被称为免疫抑制剂的药物联合使用,这些药物可以抑制患者的免疫系统。这样做的原因在于,这些细胞并不来自患者自身,因此不被认为是“本体”。如果没有免疫抑制剂的干扰,这些细胞将遭到排斥。我们的目标是找到一种通过基因工程制造的细胞,能够避免被视为外来物。我坚信这是一个可以解决的问题。为什么?当一个女人怀孕生下一个孩子时,这个孩子拥有两套基因,一套来自母亲的卵子,这些基因被身体认定为“自己的”;另一套来自父亲,这些基因则被视为“非自己的”。然而,母体的身体为何不会对胎儿产生排斥反应呢?如果我们能够找到这其中的奥秘,将有助于我们思考如何在干细胞衍生的胰岛细胞中进行基因改造,使其能够适用于任何人体。这种技术不仅关乎糖尿病,还可以应用于其他任何需要移植的细胞,包括肝脏甚至心脏,这可能意味着我们将不再需要担心免疫抑制的问题。1.Breakthrough within reach for diabetes scientist and patients nearest to his heart.The Harvard Gazette.2.Douglas A. Melton, Ph.D. Harvard University.3.Can Lab-Grown Beta Cells Revolutionize Diabetes Care?.University of California San Francisco.