Bringing medical advances from the lab to the clinic.
关键词:胎儿发育;营养控制基因;剑桥大学;Cell Metabolism
这项发表于2023年7月11日由英国剑桥大学约翰学院发表于Cell Metabolism的研究,首次直接证明父源基因影响母体将营养转移到胎儿【1】。研究人员发现,胎儿能利用来自父亲的基因Igf2操控其母亲的胎盘激素,从而在胚胎发育期间获取更多营养以满足自己的生长需求【2】。科学家发现,在小鼠的胎盘内分泌细胞中,名为Igf2的印记基因表达非常高。Igf2是一个重要的父源印记基因,控制“胰岛素样生长因子2”的蛋白表达。研究人员首先观察了Igf2基因对于胎儿发育的意义。发现这个基因类似于控制我们血液中葡萄糖水平的激素胰岛素,它促进胎儿的生长,并在胎儿组织(包括胎盘、肝脏和大脑)的发育中起着关键作用。(图1. Igf2基因的删除,导致胎儿发育受到影响)科学家发现,从胎盘信号细胞中删除Igf2会影响其他激素的产生。即,Igf2控制胎盘激素的产生,包括催乳素,并且在建立怀孕相关的胰岛素抵抗性以及分配营养给胎儿方面起着关键作用。进一步,研究人员分析了Igf2基因影响胎儿发育和母体代谢的机制。
Igf2控制蛋白质合成和细胞能量平衡,这些行为依赖于胎盘内分泌细胞类型。
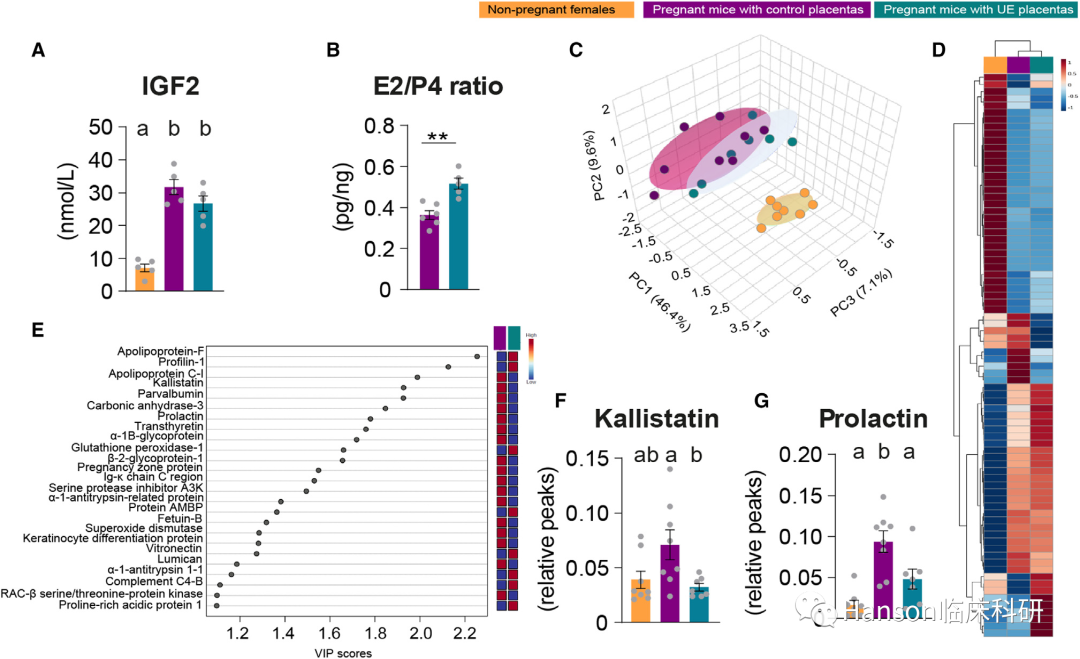
(图3. Igf2控制蛋白质合成和细胞能量平衡)
不仅如此,Igf2的缺失还会对成年后代的新陈代谢产生额外的长期影响。
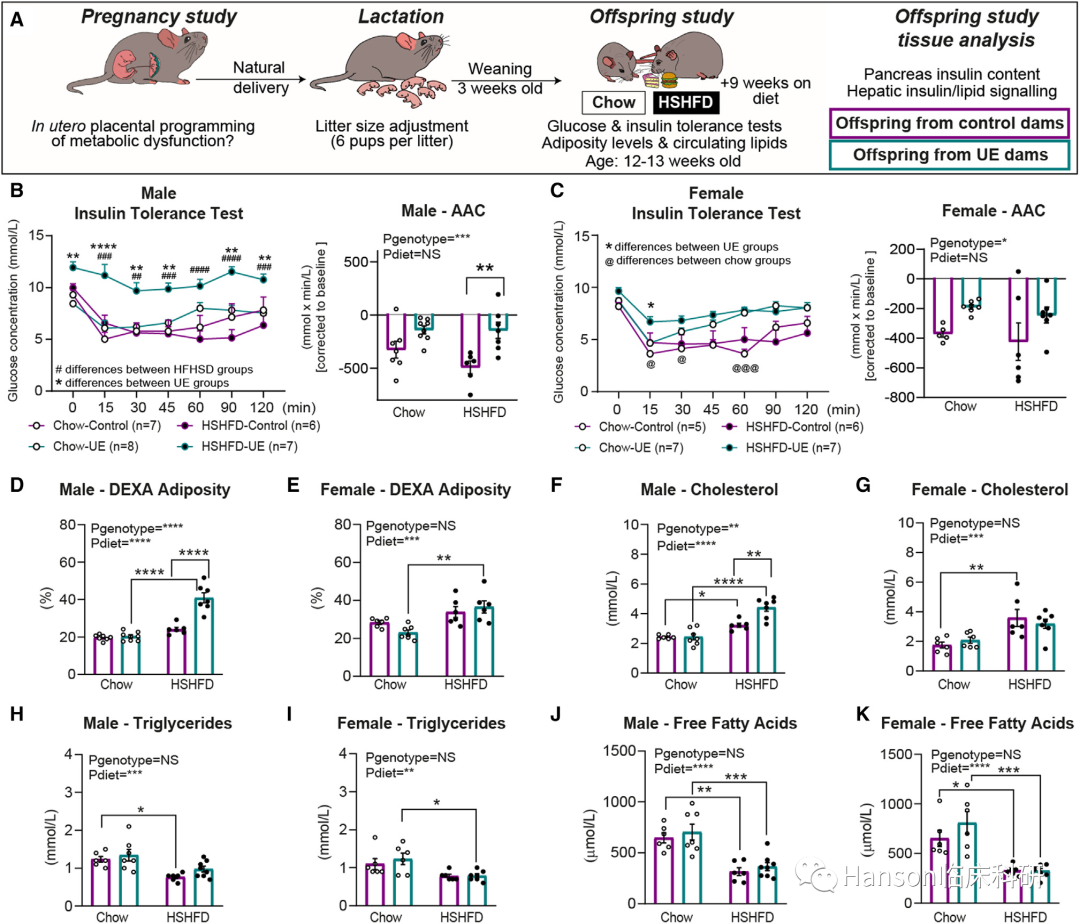
“直到现在,我们才知道Igf2基因的一部分功能是参与母体激素调节,将营养分配给胎儿,”
剑桥大学的研究让我们更清晰地理解,在胎儿发育期间父源基因和母源基因通过胎儿影响母体的代谢和胎盘激素。来自父源的基因更倾向于促进胎儿的生长;而母源基因则希望宝宝存活下来,但同时需要保持其母体的葡萄糖和脂肪水平,以维持其自身的健康,以便能够分娩、哺乳并再次生育。本研究提供了首个直接证据,显示父源的基因信号促使母体将营养转移到胎儿。科学家清晰地展示了名为Igf2的印记基因的作用:没有Igf2,母亲就不会为胎儿提供足够的葡萄糖和脂肪,导致胎儿生长不足;不仅如此,携带Igf2基因缺陷的婴儿可能会生长过大或生长受限,影响他们的终身健康,可能在以后的生活中导致糖尿病和肥胖症。下一步的研究目标是理解胎盘激素如何受Igf2控制,以及这些激素的作用。更深入的研究可能有助于科学家发现新的策略,以针对胎盘改善母婴健康状况。【1】 Lopez-Tello J, et al. Fetal manipulation of maternal metabolism is a critical function of the imprinted Igf2 gene. Cell Metab. 2023 Jul 11;35(7):1195-1208.e6. doi: 10.1016/j.cmet.2023.06.007. PMID: 37437545.【2】 https://neurosciencenews.com/paternal-genetics-baby-nutrition-23638/本公众号仅作已发表研究论文的数据分享和解读,仅供学术讨论,而不具临床指导意义。
本期编辑:Henry,微信号healsan。助理:ChatGPTHanson临床科研团队,在美国的七位生物医学科学家主持并担任独立理事。主要通过大数据分析,分享生物医学前沿、发展趋势及对临床科研的启发;通过文献计量分析及报告,把握最新技术进展;交流SCI论文撰写、课题设计规范。只提供以数据为基础的客观报告,及专业、独立的思考。
(点击👆图片,进入自己感兴趣的专辑。或获得点击“资源”,浏览本公众号所有资源。)(获取本次解读的原文,请加科研助手;并提供本次文章编号20230717)