
动脉粥样硬化是动脉壁的慢性炎症性疾病,是急性冠脉综合征和缺血性卒中的病理生理基础,也是全世界死亡和残疾的主要原因。近年来,随着血运重建技术和预防策略的发展,动脉粥样硬化及其并发症的临床管理有了很大改善。尽管如此,心血管疾病的患病率和急性事件(如心肌梗死)的发生率在过去30年中仍有所增加,患者死亡率较高。因此,亟需寻找新的靶点,以降低心血管事件风险。近日,European Heart Journal of Cardiology发表的综述对动脉粥样硬化的新机制和治疗靶点进行了汇总,本文摘录了部分要点内容,以飨读者。
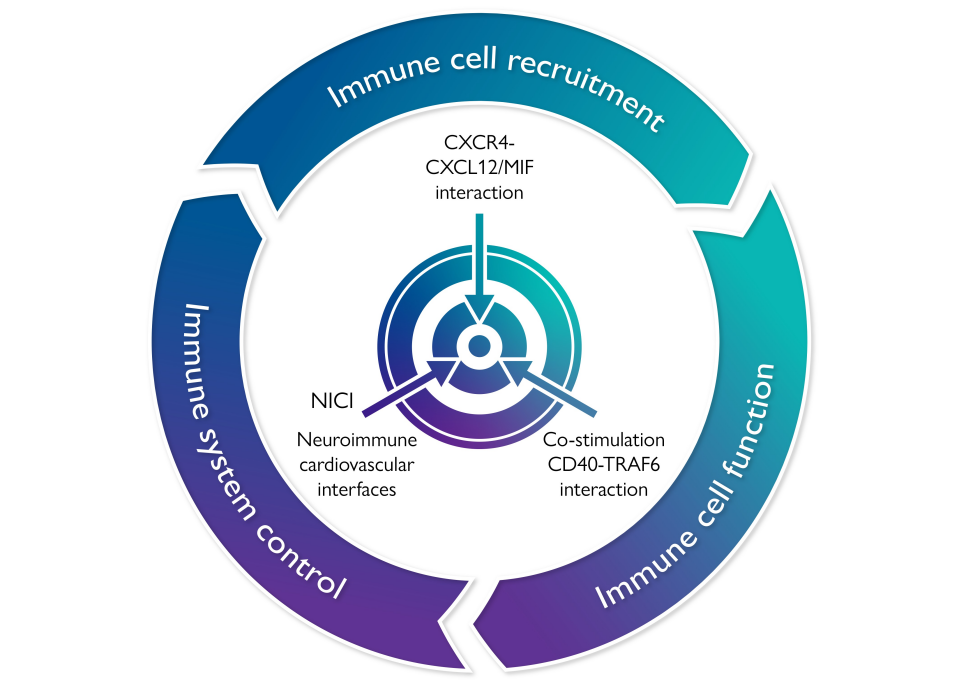
图1 中心图
肿瘤坏死因子(TNF)受体相关的信号分子CD40及其配体CD40L已被证明是动脉粥样硬化免疫反应的关键。选择性靶向CD40下游的信号分子,如巨噬细胞中的TNF受体相关因子(TRAF),可能具有更好的特异性。在缺乏特异性CD40-TRAF相互作用的转基因小鼠中发现,缺乏CD40-TRAF6(而不是CD40-TRAF2/3/5)信号通路可以消除Apoe缺陷小鼠动脉粥样硬化,并赋予斑块稳定性。在巨噬细胞中高表达的TRAF6,与代谢性炎症相关。该综述识别出两种阻断CD40-TRAF6信号传导的特异性小分子抑制剂(称为TRAF-STOPs),这两种抑制剂减少了已建立的动脉粥样硬化、有限的斑块不稳定性和单核细胞募集,同时保留了经典的cd40介导的免疫应答。在小鼠和非人灵长类动物中,包装在rHDL纳米颗粒中的TRAF-STOPs可促进巨噬细胞对其摄取,减少动脉粥样硬化。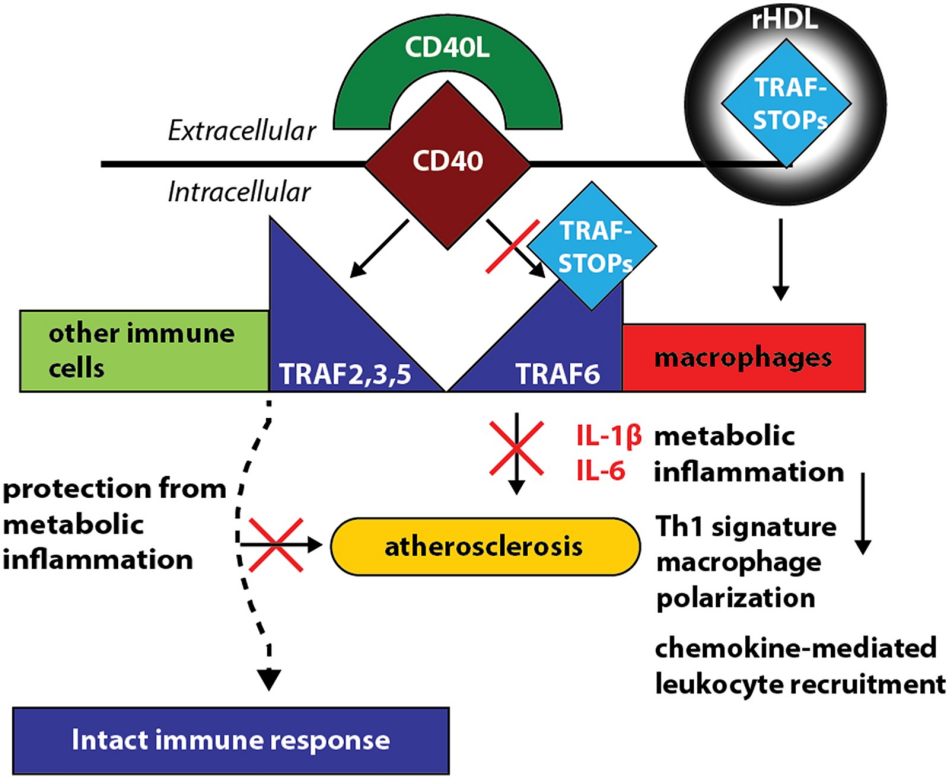 图2 TRAF-STOPs阻断CD40-TRAF6信号传导
图2 TRAF-STOPs阻断CD40-TRAF6信号传导
在动脉粥样硬化等特定的微环境中,一些趋化因子异构体(如CCL5)与CXCL4结合时变得更加活跃,通过增加动脉单核细胞募集促进动脉粥样硬化的发生。通过与相互作用基序竞争的特定肽抑制剂阻止这些异二聚体的形成,可减少小鼠动脉粥样硬化病变的形成。
通过核磁共振对各种异二聚体进行结构-功能分析,并模拟特定的肽抑制剂,发现可以通过减弱CCL5-CXCL4协同作用驱动的髓系募集,或通过增强调节性T细胞(Tregs)阻断CC型异聚体与CCL5的相互作用,预防动脉粥样硬化。一种环肽[VREY]4旨在专门靶向CCL5和CXCL12之间的相互作用,这种新颖的原理可抑制血小板活化。趋化因子受体CXCR4及其同源配体CXCL12和非同源配体MIF对胚胎血管生成和成人血管完整性至关重要。CXCL12和CXCR4在冠状动脉疾病和动脉粥样硬化中作用模式复杂。CXCL12可通过激活CXCR4,导致血小板活化,CCL5可竞争性地阻断了这一作用。i[VREY]4模拟CCL5的螺旋肽,可与活化血小板上的CXCL12和CXCR4形成复合物,并具有高亲和力,可通过调节CXCL12-CXCR4相互作用,阻断CXCL12诱导的血小板活化,从而阻断血栓形成(图3)。图3 针对CXCR4及其配体CXCL12和MIF的治疗策略
广泛的神经免疫心血管界面(NICI)出现在小鼠和人类动脉粥样硬化病变的外膜段,显示出扩大的轴突网络,包括免疫细胞和介质平滑肌细胞附近轴突末端的生长锥。小鼠NICI建立了一个结构性的动脉-脑回路。腹腔-外膜伤害性传入神经通过背根神经节进入中枢神经系统(CNS),进而投射至脑干延髓(图4A);交感传出神经元从髓质和下丘脑神经元通过脊髓中外侧神经元,和腹腔和交感链神经节投射到腹腔内(图4B)。
此外,动脉-脑回路的外周神经系统(PNS)成分被激活:脾脏交感神经和腹腔迷走神经的活动与疾病进展同步增加,而腹腔神经节切除术则导致了腹腔内NICI的瓦解,减少了疾病进展并增强了斑块稳定性。因此,PNC利用NICI组装动脉-脑回路,对动脉-脑回路的治疗干预可以减弱动脉粥样硬化,开启了动脉粥样硬化研究的新篇章。参考文献:Christian Weber, Andreas J R Habenicht, Philipp von Hundelshausen. Novel mechanisms and therapeutic targets in atherosclerosis: inflammation and beyond. Eur Heart J. 2023 Aug 1;44(29):2672-2681.
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
图2 TRAF-STOPs阻断CD40-TRAF6信号传导