高血压、糖尿病(以高血糖为特征)和血脂异常[以血清胆固醇或甘油三酯(TG)水平升高为主要表现]常统称为“三高”,是心血管疾病(CVD)发病和死亡的3项主要危险因素,且许多患者“三高”并存,导致发生严重心血管事件的风险成倍增高。“三高”共管可显著降低主要心血管事件的发生率和全因死亡率。我国患者该如何进行“三高”共管?近日发布的《“三高”共管规范化诊疗中国专家共识(2023版)》给出解答。
本共识强调以下观点:(1)高血压、糖尿病和血脂异常都是可防可控的危险因素,对“三高”应同等重视和综合管理;(2)“三高”共管的根本目标是降低发生心、脑、肾及血管并发症和死亡的总危险。应通过早期筛查和评估“三高”患病情况,结合分析其他危险因素、靶器官损害和临床合并疾病,对患者进行心血管总体风险的评估和分层,并个体化地选择管理目标;(3)构建“三高”共管上下级联动体系,实施符合我国国情的规范化的“三高”全程管理和分层管理。目前,我国≥18岁成人的高血压、糖尿病和血脂异常患病率分别为27.9%、12.4%和40.4%。“三高”常常合并存在,湖北省对35~75岁城乡居民的调查(64151人)显示,“三高”共患率为8.9%。中国2型糖尿病患者血糖、血压和血脂研究显示,29.8%的门诊糖尿病患者同时合并有高血压和血脂异常,但仅5.6%的患者经治疗实现了“三高”达标。高血压、糖尿病和血脂异常均是CVD的独立的主要危险因素。“三高”并存时,这三项危险因素相互影响、相互加重,产生协同作用,诱发和加速动脉粥样硬化、血管内皮功能异常、炎症过程和靶器官损害,成倍增加发生心血管事件和死亡的风险。实现“三高”共管的第一步是通过测量血压、血糖和血脂指标检出高血压、糖尿病和血脂异常患者,并确定是否为“三高”并存。然后,对患者进行总体心血管风险的评估和分层,在此基础上确立适合患者的血压、血糖和(或)血脂控制目标值,确定启动药物治疗的时机,优化治疗方案和进行综合管理(图1)。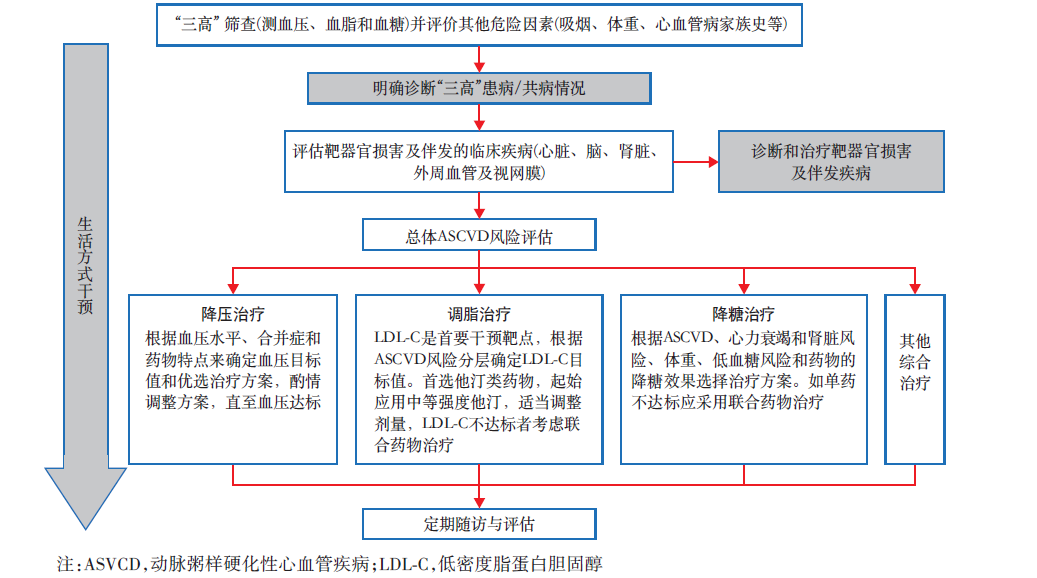 图1 “三高”共管路径大多数高血压、糖尿病和血脂异常患者无明显临床表现,需通过筛查才能早期发现。“三高”的诊断标准见图2。个体发生CVD危险的高低不仅取决于单个危险因素,如血压、血糖或胆固醇水平的高低,还取决于同时存在的其他危险因素的数目和水平、靶器官损害和临床并发症。因此,应根据三高水平、其他危险因素、靶器官损害和伴发临床疾病等情况,对患者进行心血管风险分层,并制定个体化的血压、血脂和血糖管理目标,如图3。
图1 “三高”共管路径大多数高血压、糖尿病和血脂异常患者无明显临床表现,需通过筛查才能早期发现。“三高”的诊断标准见图2。个体发生CVD危险的高低不仅取决于单个危险因素,如血压、血糖或胆固醇水平的高低,还取决于同时存在的其他危险因素的数目和水平、靶器官损害和临床并发症。因此,应根据三高水平、其他危险因素、靶器官损害和伴发临床疾病等情况,对患者进行心血管风险分层,并制定个体化的血压、血脂和血糖管理目标,如图3。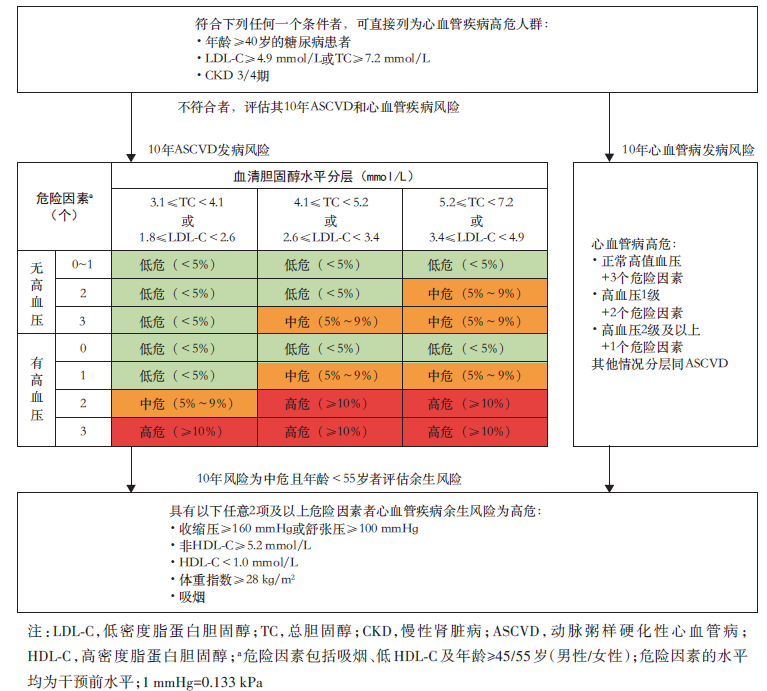 图3 中国成人心血管病一级预防风险评估流程图“三高”患者需综合管理,将血压、血糖和血脂等临床指标尽可能控制在目标值范围内。本共识推荐的“三高”患者的各项临床指标控制目标值见图4。在临床实践中,应遵循个体化原则来实现这些指标的目标值,综合考虑患者的年龄、意愿、预期寿命、病程长短、有无并发症和治疗反应等因素。尤其是在血糖管理时,对老年患者,低血糖高风险患者,病程较长、预期寿命较短、有严重并发症或合并症的患者,可采取相对宽松的空腹血糖、非空腹血糖或HbA1c目标值(例如HbA1c可放宽至<8%)。生活方式干预在任何时候对任何“三高”患者都是合理、有效的治疗,其改善血脂异常和降低血压、血糖以及心血管风险的作用肯定,所有患者都应采用。
图3 中国成人心血管病一级预防风险评估流程图“三高”患者需综合管理,将血压、血糖和血脂等临床指标尽可能控制在目标值范围内。本共识推荐的“三高”患者的各项临床指标控制目标值见图4。在临床实践中,应遵循个体化原则来实现这些指标的目标值,综合考虑患者的年龄、意愿、预期寿命、病程长短、有无并发症和治疗反应等因素。尤其是在血糖管理时,对老年患者,低血糖高风险患者,病程较长、预期寿命较短、有严重并发症或合并症的患者,可采取相对宽松的空腹血糖、非空腹血糖或HbA1c目标值(例如HbA1c可放宽至<8%)。生活方式干预在任何时候对任何“三高”患者都是合理、有效的治疗,其改善血脂异常和降低血压、血糖以及心血管风险的作用肯定,所有患者都应采用。生活方式干预的主要措施包括:
(1)合理膳食,建议高血压患者采用DASH或中国心脏健康饮食;
(2)减少钠盐摄入,每日食盐不超过5 g;
(3)增加身体运动,减少久坐等静态生活方式,每周至少150 min中等强度身体运动;
(4)控制体重,使体重指数<24 kg/m²,男性腹围<90 cm、女性腹围<85 cm;
(5)不吸烟、彻底戒烟、避免被动吸烟;
(6)不饮酒或限制饮酒;
(7)减轻精神压力,保持心理平衡;
高血压治疗的根本目标是降低发生心脑肾及血管并发症和死亡的总危险。在改善生活方式的基础上,应根据患者的总体风险水平选择降压药物,实现血压达标;同时干预可纠正的危险因素、靶器官损害和并存的临床疾病,降低总体心血管事件和全因死亡的风险。血管紧张素转换酶抑制剂(ACEI)、血管紧张素Ⅱ受体拮抗剂(ARB)、钙通道阻滞剂(CCB)、利尿剂、β受体阻滞剂和血管紧张素受体脑啡肽酶抑制剂(ARNI)均可作为一线降压药物,应根据患者的血压水平和心血管风险水平选择初始单药或联合治疗。对血压≥160/100 mmHg、高于目标血压20/10 mmHg的高危患者,或单药治疗未达标的高血压患者,应进行联合降压治疗,包括药物自由联合或单片复方制剂(SPC),从改善治疗依从性和持续性的角度可考虑优先应用SPC(图5)。优先选择一日一次的长效降压药物,以有效控制24 h血压。管理血压的同时还应兼顾心率,对高血压伴持续性心率增快的患者(静息心率>80次/min),应考虑使用β受体阻滞剂,首选β1受体阻滞剂如琥珀酸美托洛尔缓释片或比索洛尔。对确诊的2型糖尿病患者,在饮食管理和运动治疗的同时,应及时启动降糖药物治疗。应选择安全、有效、能使血糖达标并维持达标的降糖药物,二甲双胍是大多数2型糖尿病患者控制高血糖的一线用药和药物联合中的基本用药。超重和肥胖的患者可优先考虑能减轻体重的降糖药物。ASCVD患者、心血管病高危患者、心力衰竭患者和(或)CKD患者,治疗方案中应包括能降低心肾风险的药物,如钠-葡萄糖共转运蛋白2 抑制剂(SGLT2i)和(或)胰高糖素样肽-1受体激动剂(GLP-1 RA)(图6)。糖尿病合并CKD的患者需强化综合管理,包括中等强度他汀或联合其他降脂药物治疗。降糖药物通常首选SGLT2i和(或)GLP-1 RA。合并高血压和蛋白尿的患者应使用一种ACEI或ARB, 并将剂量上调至能耐受的最大剂量。估算肾小球滤过率(eGFR)≥25 ml/min/1.73 m²、有蛋白尿且血钾正常的2型糖尿病患者,可考虑使用已证实对心肾有益的非甾体类盐皮质激素受体拮抗剂非奈利酮。经足量口服降糖药物联合治疗后HbA1c不能达标的患者,可开始口服药和注射降糖药(GLP-1RA或胰岛素)的联合治疗。有高血糖症状(如多尿或多饮)、持续分解代谢证据(如出现无明显诱因的体重显著下降)、HbA1c(>10%)或血糖(>16.7 mmol/L)水平很高的患者,考虑尽早启动胰岛素治疗。LDL-C是降脂治疗的首要干预靶点,非HDL-C可作为次要干预靶点。LDL-C降得越低,维持LDL-C低水平的时间越长,ASCVD风险下降越显著。目前,各国指南推荐根据个体的ASCVD风险分层来决定LDL-C的目标值(图4)。临床上,可供选用的降脂药物大体上可分为2大类:①主要降胆固醇的药物,包括他汀类、胆固醇吸收抑制剂、前蛋白转化酶枯草杆菌蛋白酶/kexin 9型(PCSK9)抑制剂及其他降脂药(胆酸螯合剂等)。②主要降TG的药物,包括贝特类、烟酸类和高纯度omega-3脂肪酸。部分降脂药物兼有降低胆固醇、降低TG和/或改善其他血脂成分的作用。对于严重的高脂血症,常需多种降脂药物联合应用,才能获得良好疗效。他汀类药物是首选的降脂药物,一般推荐起始应用中等强度他汀(可降低LDL-C水平25%~50%),根据个体的降脂疗效和耐受情况,适当调整剂量;若LDL-C不能达标,建议联用胆固醇吸收抑制剂;如LDL-C仍不达标,应加用PCSK9抑制剂。对血清TG水平增高(≥1.7 mmol/L)的患者,首先应用非药物干预措施。TG≥2.3 mmol/L者可考虑在他汀治疗基础上加用贝特类或高纯度omega-3脂肪酸。对于严重高TG血症患者(TG≥5.7 mmol/L),为降低急性胰腺炎风险,应首先考虑使用主要降低TG的药物(图7)。“三高”患者合并冠心病、CKD、心力衰竭等疾病时,应根据相关指南对这些疾病进行综合性的优化管理和治疗。除此之外,要实现“三高”共管还需要统筹各方资源,健全政府主导、部门协作、动员社会、全民参与的慢性病综合防治机制,实现“三高”共管的分层管理。